Ein Gastbeitrag von Dr. Uwe Peters
Vergleiche – Gemeinsamkeiten und Unterschiede
Angesichts der enormen Beachtung, die im Moment die Ausbreitung eines Corona-Virus über die Welt erfährt, stellen sich viele Fragen über unser gesichertes Wissen zu Viren. Analysiert man die Entscheidungsbasis für die gravierenden Maßnahmen, dann stellt man bei der nüchternen Betrachtung fest, dass die so wissenschaftlich und rational daherkommenden Argumente zum einen auf einer extrem einseitigen Betrachtung und zum andern auf einer extrem dünnen Datenbasis beruhen. Der immer wieder „untersagte“ Vergleich mit der Influenza, wird aber auch in Kreisen der Virologen herangezogen, wenn es um die Abschätzung der Entwicklung des Corona Virus geht. Ein Vergleich bedeutet ja nicht, dass die Dinge gleich sind, sondern ein Vergleich dient dazu Gemeinsamkeiten und Unterschiede herauszuarbeiten und zu bewerten, um den Grad der Ähnlichkeit zu ermitteln und zu bewerten.
In aller Kürze:
Beides, Grippe und Covid-19, die vom neuen Corona-Virus (CoV2) ausgelöste Erkrankung, sind Erkrankungen der Atemwege, die vor allem bei älteren Menschen zum Tode führen. Auffällig ist, dass bei der Grippe zwar überwiegend alte Menschen betroffen sind, aber das Durchschnittsalter der Influenza-Toten etwas niedriger ist (zwischen 75 und 77 Jahren; Covid-19 derzeit 81 Jahre). Das weist darauf hin, dass es bei der Influenza mehr tödliche Verläufe auch bei Menschen im jungen und mittleren Lebensalter gibt (Covid19 – keine 100 Toten in der Altersgrupp 0 – 50 Jahre von 7000 Gestorbenen in Deutschland). Die Anzahl invasiv beatmungspflichtiger Menschen ist bei der Influenza geringer. Die Sterblichkeit aber durchaus vergleichbar. Das Thema Folgeerkrankungen wird gerade diskutiert. Für die Influenza ist bekannt, dass schwere bakterielle Folgeerkrankungen ein großes Problem darstellen, die z.T. tödlich verlaufen oder die Rekonvaleszenz über Wochen beeinflussen (https://link.springer.com/chapter/10.1007/82_2014_394).
Was die Ausbreitung und Ausbreitungswege betrifft sind Verläufe durchaus vergleichbar, und es wurden zur Abschätzung der Modelle u.a. Influenza Pandemien herangezogen. Ausgangspunkt für die Modelle sind häufig die Abläufe in der spanischen Grippe und die Annahme, dass es zu ähnlichen Zuständen kommen könnte.
Corona – eine Pandemie im Licht der Statistik
Von der Pandemie blieben 99.9% der Menschen verschont, obwohl noch nie so viel auf einen Virus getestet wurde: über 60 Millionen Tests an Menschen mit Atemwegssymptomen, die in über 90% negativ ausgefallen sind. Nahezu alle Menschen (fast 90 %), die starben, waren multimorbide (oft stark übergewichtig mit BMI >35 und Raucher), hochbetagt und zumeist in Pflege. Es waren Menschen, die auch sonst zumeist an Infekten der Atemwege versterben, egal ob viral oder bakteriell bedingt. Hier spielt die infektiologische Ökologie eine Rolle, auf die ich im Weiteren eingehen möchte.
Menschliche Schicksale in Zahlen zu fassen ist immer problematisch. Um Abwägungen von Maßnahmen und Einsatz von endlichen Ressourcen vernünftig vornehmen zu können sind solche Betrachtungen aber unvermeidlich. In England ist dies tägliche Routine, für Krebskranke stehen hier 40.000 Pfund zur Verfügung, um ein sog. qualifiziertes Lebensjahr zu erreichen. In Deutschland wird diese Bewertung flexibler gehandhabt, aber rund 100.000 € pro Jahr gilt als Zielvorgabe. (https://www.tagesspiegel.de/wissen/krebsbehandlung-160-000-euro-pro-lebensjahr/1045720.html)
Nun zurück zu Covid-19:
Jährlich sterben auf der Welt rund 70 Millionen Menschen. CoV2 hat in 100 Tagen 350.000 Opfer gefordert, so viele also, wie sonst an 1,5 Tagen sterben. In der gleichen Zeit sind etwa 200.000 Menschen an multiresistenten Bakterien gestorben (700.000 im Jahr), davon allein in Deutschland 20.000 (https://www.tagesschau.de/inland/infektionen-101.html). In den Tagen der Corona-Pandemie sind ca. 3 Millionen Menschen auf der Welt verhungert. Wenn die Schätzungen stimmen sind das rund 15 % mehr als im Vorjahr.
Solche Aspekte und Relationen wurden in den Beschlüssen zu den ergriffenen Maßnahmen aber vollkommen ausgeblendet. Nur die panikverbreitenden Modelle der „Pandemiker“ wurden betrachtet. Dabei vereint alle Modelle eine Eigenschaft: Sie waren bisher immer falsch! Seit Mitte der 90er Jahre wurden zahlreiche Influenza-Szenarien veröffentlich, die vor mehreren Millionen Toten weltweit warnten. Vogelgrippe, Schweinegrippe, SARS, MERS, und Ebola – alles virale Bedrohungen, die zu Millionen Toten führen sollten. Die Zahlen in der Realität waren meist um den Faktor 100-1000 niedriger.
Am 26.3.2020 schrieb die pharmazeutische Zeitung (https://www.pharmazeutische-zeitung.de/vorsicht-bei-vergleich-der-zahl-der-todesfaelle-116540/) Zitat: „Im Iran, wo lange keine Schutzmaßnahmen ergriffen wurden, rechnen Forscher laut einem »Spiegel online«-Bericht jetzt mit bis zu 3,5 Millionen Toten. Das Land hat in etwa gleich viele Einwohner wie Deutschland, rund 82 Millionen.“ An diesem Tag wurden im Iran 3.000 Fälle pro Tag gezählt, in Deutschland waren es bereits über 6.000. Am 17.5.2020 hat der Iran aber, gleichauf mit Deutschland, den Tod von 6.000 vor allem alten Menschen zu beklagen. Vorhersage zu Realität: 500:1.
Die Modellfehler sind in der Wissenschaft hinlängliche bekannt, unverständlich ist nur warum den Beteuerungen der Virologen, dass sie – jetzt endlich – realitätsnah wären (Podcast Christian Drosten, Mitte März 2020) in einem solchen Umfang Glauben geschenkt wird.
Von Viren und Virenträgern
Auf ein virales Geschehen kann man unter verschiedenen Aspekten blicken. Uns Mediziner interessiert, wie die Krankheit bei Patienten verläuft und wie wir heilend eingreifen können. Zudem steht bei ansteckenden Erkrankungen die Frage im Raum, wie die Ansteckung eingedämmt werden kann. Dabei sind dann die Fragen der Übertragungswege und die Eigenschaften des Erregers wichtig. Vor allem für Bakterien haben wir hier gute Daten zur Verfügung.
In Bezug auf Viren beginnt dann aber eine ganze Kaskade von Interpretationen von denen wir im Moment lernen, dass sie zu Fehlschlüssen führen. Und das CoV2-Modell reiht sich in seinen Aussagen in die Reihe dieser Fehlschlüsse nahtlos ein. Denn virale Erkrankungen verhalten sich in der Ausbreitung offensichtlich anders als die Erkrankungen bakteriellen Ursprungs. Die erste ungeklärte Frage ist die Übertragung der Viren. Die Suche nach dem Patienten „Null“ könnte sich als der vollkommen falsche Ansatz erweisen.
Wie werden Viren übertragen?
Hierzu gibt es aus dem Bereich der Influenza zahllose Veröffentlichungen. Je nach Autor und Modell ist es der Luftstrom der Atemluft oder die Tröpfchen, die beim Niesen oder Husten in die Luft abgegeben werden. Der Faktor kontaminierte Oberflächen, von denen der Virus durch die Hand aufgenommen wird, scheint vor allem bei Viren des Respirationstraktes die kleinere Rolle zu spielen, anders bei Darminfektionen. Bei allen Betrachtungen bleibt es überwiegend beim Fokus auf die Mensch-zu-Mensch-Interaktion: Globaler Reiseverkehr, öffentlicher Nahverkehr, Gedränge, Fußballstadien. Bei Corona diskutieren wir Ischgl, Karneval und Traditionsfeste als „Brandbeschleuniger und Hotspots“. Aber hatten St. Anton oder andere Skiorte keine Feiern gehabt, wie Ischgl? Wurde nur in Heinsberg und nicht auch in Mainz und andernorts Karneval gefeiert? Wie weit trägt hier die Kausalkette? Aber Monokausalität ist praktisch, da sie sehr einfach nachzuvollziehen ist. Leider wissen wir von der Influenza, dass nach den Karnevalsfeiern die Arztpraxen voll sind, aber Fußballstadien nur selten zur Quelle einer Infektwelle werden.
Welche Daten brauchen wir?
a) Übertragungswege
b) Infektiosität (Dosis an Viren die 50% der Menschen infiziert)
c) Überlebenszeit in aktiver Form außerhalb des Menschen
Dies gilt für die aktiven Formen im unmittelbaren Umfeld. Für Covid-19 liegen dazu eine Reihe von Schätzungen und widersprüchlichen Daten vor, jedoch keine verlässlichen Studien.
Der andere Blick auf die Viren
Die Übertragungswege von Viren sind aus ökologischer Sicht jedoch in einem ganz anderen Licht zu betrachten. Der Anteil der Mensch zu Mensch-Übertragung spielt unbestritten eine Rolle, nur ist die Frage in welchem Umfang. Vielleicht sind es vor allem die aktiven Formen, die über diesen Weg zu schnell ansteigenden Fallzahlen in einzelnen Regionen führen.
Aber wie erklären wir darüber die pandemische Ausbreitung? Megastädte, Flugverkehr, hohe Einwohnerdichte – der Faktor Globalisierung als todbringendes Risiko? Eher nein, denn Pandemien gibt es schon seit langem: allein die Influenza begleitet die Menschheit bereits mehrere Jahrhunderte. Auch die Pandemie 1918 hat sich trotz fehlenden Flugverkehrs und nur 15 Städten mit mehr als einer Million Einwohner (heute über 300) nahezu genauso schnell über die Welt verbreitet, wie heutige Wellen. Wie das den Viren gelingt ist bisher vollkommen ungeklärt. Die ökologische Virenforschung liefert erste Ansätze: Untersuchungen zeigen, dass das Grundwasser (https://www.sciencedirect.com/science/article/abs/pii/004313548990095X), die Luft und Vektoren, wie Bakterien und Pilze (https://www.sciencedirect.com/science/article/pii/B9780444887283500160), eine größere Rolle spielen als bisher gedacht.
Die Vorstellung, dass humanpathogene Viren mit Vögeln oder deren Bakterien reisen ist nicht abwegig. Dabei spielt für die Ausprägung der Infektionsrate das Verhältnis von aktiven zu inaktiven Virusformen eine besondere Rolle, wie schon in den 40er Jahren an Abwasserexperimenten mit Affen zur Erforschung der Polio-Infektion gezeigt wurde (Environmental virology: from detection of virus in sewage and water by isolation to identification by molecular biology—a trip of over 50 years). Der Weg der Viren durch die Stratosphäre in 2.000 –3.000m Höhe ist heute ebenfalls unbestrittener Fakt (https://www.nature.com/articles/s41396-017-0042-4).
Ein Blick auf die Corona-Verbreitungskarte von Schweden ist in diesem Zusammenhang interessant. In Norrbotten leben ca. 10 Menschen/km2 und „social distancing“ ist immer schon ein Teil des Lebens in dieser Region. Dennoch beträgt die Anzahl Corona-Fälle pro 100.000 Einwohner etwa 130 und verteilt sich über die große Fläche (Abb. 1).
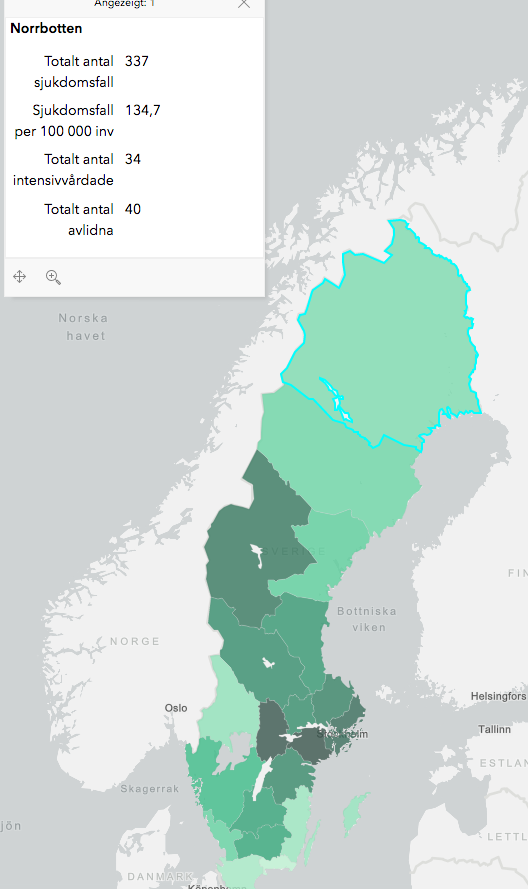
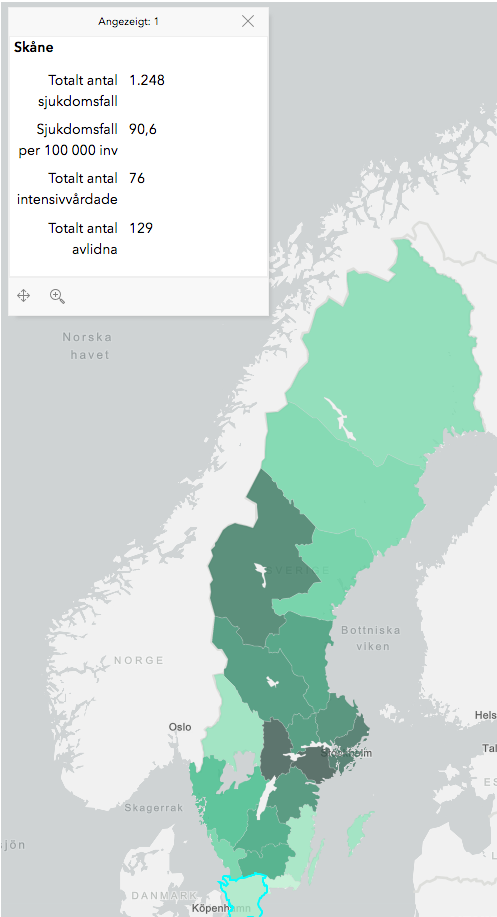
In Skåne ist die Einwohnerdichte rund 10mal höher, dort liegen die beiden Städte Lund und Malmö, in denen das Leben mit geöffneten Restaurants, Schwimmbädern und Saunen, Sportveranstaltungen, Geschäften ohne Begrenzung und Mund-Nasenschutz weiterlief. Die Fallzahl liegt bei 90 CoV2-Fällen/100.000 Einwohnern. Hier stellt sich die Frage der Plausibilität von rein auf Mensch-zu-Mensch fokussierten Verbreitungsmustern. Das Ausmaß der Infektiosität ist bisher für CoV2 auf einer evidenzbasierten wissenschaftlichen Weise nicht geklärt. Die meisten Untersuchungen sehen dies als eine Eigenschaft des Virus. Dies lässt die Wirt-Erreger-Interaktion aber vollkommen außer Acht. Und bleibt man im virologischen Modell, dann kann schon jetzt für CoV2 postuliert werden: Die Infektiosität in den Altersklassen variiert stark. Menschen unter 40 scheinen von dem Virus deutlich seltener betroffen zu sein, da die Nachweisrate in den durchgeführten Test in diesen Altersgruppen weit geringer ist, als in der Gruppe der 50-70-Jährigen. Daten zur Manifestationszahl in den Altersklassen sind derzeit nicht bekannt und schwanken zwischen 50-90%.
Zudem ist unklar, in welchem Ausmaß und zu welchem Zeitpunkt Menschen für andere infektiös sind. Bei den meisten Virusinfektionen ist eine hohe Ansteckungswahrscheinlichkeit in den ersten Tagen nach Auftreten der Symptome gegeben, da in dieser Phase die meisten Viren aus den befallenen Zellen freigesetzt werden. Ob symptomlose Menschen wirklich andere Menschen mit Corona anstecken können ist derzeit trotz aller Vermutungen in diese Richtung wissenschaftlich unklar. Was den Kontakt zu anderen Menschen im normalen Alltag betrifft, so scheint es aber eher unwahrscheinlich zu sein. Für Alten- und Pflegeheime mag dies u.U. anders aussehen. Gegen die Theorie der Übertragung durch symptomlose Menschen spricht zudem die Tatsache, dass der Virusnachweis in Aerosolen durch Niesen nicht gelang, im Speichel und Sputum nur vereinzelt.
Sicher ist nur ein Rachenabstrich mit Zellmaterial. In diesen Zielzellen vermehrt sich das Virus zunächst und die Virenfreisetzung unter Zerstörung der Zellen verursacht die symptomauslösende Immunreaktion. Zu diesem Zeitpunkt sind dann Viren in großer Zahl in der Atemwegsschleimhaut. Das ist für die gängigen Atemwegsviren bekannt, und dass dies für CoV2 anders sein könnte, ist derzeit lediglich ein Postulat. Hier stoßen wir auf ein generelles Problem: eine auf gesicherten wissenschaftlichen Daten basierende genaue Beschreibung der Übertragungswege gibt es bei fast allen Viren derzeit nicht. Die infektiöse Virusdosis ist unbekannt, die Überlebensdauer aktiver Virusformen auf Händen und Oberflächen ebenfalls.
Somit stellt sich die Frage: Auf welcher Datengrundlage wurden daher strafbewährte (also bei Zuwiderhandlung mit Strafe bedrohte) Maßnahmen wie Mund-Nase-Schutz und Kontaktverbote ausgesprochen?
Der „Rundum-Blick“ auf Viren
Die „Daseinsform“ Virus ist nach wie vor für uns nicht fassbar. Eine spannende Frage ist: Warum bilden bestimmte Körperzellen Rezeptoren aus, die dem Virus die Chance geben anzuheften? CoV2 an den Lungenzellen, FSME an den Nervenzellen usw. Hier kommt die Evolution ins Spiel. Viren sind ein zentraler Motor der Evolution. Das menschliche Genom besteht zu zweistelligen Prozentzahlen aus Resten von Virus-DNA (https://www.museumfuernaturkunde.berlin/de/ueber/neuigkeiten/viren-krankheitserreger-und-beschleuniger-der-evolution). Gerade gekapselte Viren brauchen immer einen Wirt, um die „dritte Schutzschicht“, nämlich die Kapsel aus Membranteilen des Wirtes zu erhalten. Wie diese erstmal „inaktiven“ Viren dies in einem ersten Schritt bewerkstelligen, ist Gegenstand interessanter Forschungsprojekte (https://www.sciencedirect.com/science/article/abs/pii/S0959440X05002216).
Was man daraus ableiten kann ist, dass vor allem die Viren, die sich mit einer passenden Membran umgeben haben, in das Muster der Ausbreitung von Mensch zu Mensch passen. Viren, die noch über keine passende Hülle verfügen, haben daher deutlich schlechtere Startbedingungen und das körpereigene Immunsystem hat bessere Chancen, die Virenlast zu senken, bevor es zur Erkrankung kommt. Das würde bedeuten, dass Hotspots mehr oder minder von einer Reihe Zufallsfaktoren abhängen, bevor die Mensch-zu-Mensch Infektionskette beginnt (Vgl. Nord und Südschweden). Hinzu kommt, dass die Pathogenität von vielen Viren bei jedem „Durchgang“ durch den Wirt abnimmt. Dieses Verhalten nutzen wir bei der Attenuierung von Viren zur Impfstoffherstellung. Auch hier ist Schweden ein gutes Beispiel. Obwohl es dort eine höhere Zahl Neuinfizierter gibt als in einigen anderen europäischen Ländern, sinkt dennoch parallel die Zahl der Menschen, die im Krankenhaus behandelt werden müssen, stark.
Im Ländervergleich wird viel über die Maßnahmen und deren Wirkung diskutiert. Ein Blick auf die Sterblichkeit der Grippewellen der letzten Jahre zeigt, dass dies ein zufallsbedingtes multifaktorielles Geschehen ist, das weder über Maßnahmen, noch den Zustand des Gesundheitssystems, noch mit der Hotspot Theorie zu erklären ist. Dass Bayern wegen seiner Nähe zu Österreich und Italien besonders betroffen war, ist nur ein hilfloser Erklärungsversuch zur Rechtfertigung geschlossener Grenzen. Die Grippewelle 2016/2017 verursachte in Portugal, Spanien und Norwegen eine Übersterblichkeit. Deutschland, Schweden und Italien zeigten in diesen Jahren kaum eine Übersterblichkeit. Ganz anders 2017/2018, als Frankreich, die Beneluxstaaten, Deutschland und Schweden von der Influenza besonders betroffen waren.
Alles was solche Datenreihen zeigen ist, dass wir die Mechanismen nicht verstehen, die in der Ausbreitung und Selbstlimitierung von Viren bestehen. Gerade letzterer Punkt wurde von der vielzitierten israelischen Studie in die Diskussion eingebracht. Viren sterben nicht erst aus, wenn alle Menschen immun sind, sondern haben einen begrenzten meist kurzzeitigen Lebenszyklus in einer Infektionsphase. Wir wissen wenig über den Rückzugsraum, den die Viren dann nutzen und noch viel weniger über Mechanismen einer Reaktivierung. Die einfache Erklärung über einzelne Umweltfaktoren (Temperatur, Luftfeuchte, usw.) kann das Geschehen derzeit nur sehr lückenhaft abbilden. Die Überlebensstrategien sind offensichtlich vielfältig. Kapselfreie Viren, wie Masern, sind sehr stabil und gewähren daher die Chance einer langfristigen Immunität nach durchlebter Erkrankung und Impfung. Andere, kapseltragende, Viren wie die Influenza oder Coronaviren, sind in ihren Oberflächenstrukturen sehr wechselfreudig und vielgestaltig, was Impfstrategien erschwert.
Der wichtigste Faktor – die Mensch-Virus-Interaktion
Wenn Viren auftreten, erkranken nie 100% der Menschen, die mit dem Virus in Kontakt kommen. Zahlreiche Experimente mit Rhinoviren haben gezeigt, dass nur ein kleiner Teil der Probanden schwerwiegend erkrankt. Die meisten Probanden entwickeln Symptome, doch über ein Drittel der Probanden bleibt in der Regel völlig symptomfrei. Beobachtungen von Ausbrüchen von Infektionserkrankungen, die gut nachvollziehbar sind, zeigen ein ähnliches Ergebnis.
Beispielhaft ist hier ein lokaler Mumpsausbruch (https://www.sciencedirect.com/science/article/pii/S0264410X12006299?via%3Dihub). Die Autoren zeigten, dass 44 % der Ungeimpften und 13 % der Geimpften von der Infektion betroffen waren. Ein enger bis intimer Kontakt auf der Studentenparty war der primäre Risikofaktor. Im Studentenheim eng mit über 15 Personen zusammenzuleben erhöhte das Risiko dagegen nur geringfügig. Hieran zeigt sich, dass die individuelle Abwehrstärke eine wichtige Rolle spielt. Dieser Faktor wird häufig völlig außer Acht gelassen und in den Modellrechnungen nicht berücksichtigt.
Aber selbst mit diesem Manko erklären die Autoren einer klassischen Influenza-Modellrechnung, dass zahlreiche der jetzt diskutierten Maßnahmen nur wenig zur Eindämmung beitragen könnten.
„Next, the researchers used their model to show that strict travel restrictions would have little effect on pandemic evolution. More encouragingly, their model predicts that antiviral drugs would mitigate pandemics of a virus with an R0 up to 1.9 if every country had an antiviral drug stockpile sufficient to treat 5% of its population.“
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC1779816/
Die Wissenschaftler bringen zum Ausdruck, dass Reisebeschränkungen kaum Auswirkungen haben. Die Autoren sehen in der präventiven antiviralen Arzneimitteltherapie den besten Weg zur Eindämmung der Pandemie und dazu reiche bereits eine Versorgung von 5% der Bevölkerung. Die Autoren zeigten sogar, dass internationale Zusammenarbeit und die flächige Verteilung der Arzneimittel wirksamer ist als nationale Lösungen, selbst wenn in letzterem Fall in wenigen Staaten ein größerer Anteil der Bevölkerung versorgt werden könnte.
Wenn man sich jetzt von dem Gedanken löst, dass eine antivirale Therapie nur auf einem Arzneimittel beruht, das den Virus „tötet“, ergeben sich vollkommen neue Möglichkeiten. Antivirale Prävention ist auch die Stärkung der Abwehrleistung des potentiellen Wirtes.
Dazu ist eine ganze Reihe von Maßnahmen bekannt. Andere Ansätze kommen aus der Forschung zu Phagen. Phagen sind Viren, die Bakterien befallen, sich in ihnen vermehren und schließlich das Bakterium auflösen. Solche Viren befinden sich in der Umwelt und in unserem Darm. Die Erbinformation dieser Viren nennt man Virom. Neben dem Mikrobiom rückt zunehmend dieses Virom mit zahlreichen Phagen in den Blickpunkt. So können Phagen aus dem Darm offensichtlich mitunter Rezeptoren für pathogene Viren blockieren. Diese Virusrezeptoren sind bedeutsam für die Anheftung der Viren, dem ersten Schritt der Krankheitsauslösung. Hier wird auch in Richtung Influenza geforscht (https://www.hu-berlin.de/de/pr/nachrichten/maerz-2020/nr-20330-1). Ob und inwieweit wir das natürliche Schutzpotential nutzen können, bleibt abzuwarten, aber es sieht vielversprechend aus.
Wenn wir an Altbewährtes denken, dann wären u.a. Daten zum Thema Vitamin D-Versorgung bei Influenza und Covid-19 hochspannend und wichtig zu berücksichtigen (https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6121423/ und https://pubmed.ncbi.nlm.nih.gov/32252338/). Eine einfache und preiswerte Methode wäre z.B. gewesen, die Bewohner von Alters- und Pflegeheimen sowie Risikogruppen entsprechend zu versorgen.
Der gerne vorgebrachte Einwand der mangelnden Evidenz solcher Supplementierungen verbietet sich mittlerweile, angesichts der Fülle an nicht-evidenten und trotzdem angeordneten und bußgeldbewährten Maßnahmen. Das heißt auch, dass dringend Forschungsmittel aufgewendet werden müssen, um den Ansatz einer Stärkung der körpereigenen Abwehr weiter zu erforschen und dann effektiv bei künftigen Pandemien zum Einsatz zu bringen.
Der Vorteil einer dann weitgehend symptomlosen Virusausbreitung ist die schnelle Erreichung einer Herdenimmunität, die Beschleunigung des Prozesses der Attenuierung und die damit schnellere Erschöpfung der viralen Aktivität. Die Phytopharmazie und die Mikrobiomforschung bieten eine ganze Reihe von erfolgsversprechenden Ansätzen, die von Viren initiierten Immunreaktionen (Cytokinsturm) besser unter Kontrolle zu bringen und damit die Anzahl schwerer Krankheitsverläufe erheblich zu reduzieren. Diese Ansätze wären bei der jetzigen CoV2-Pandemie vor allem bei der Altersgruppe zwischen 45 und 65 angezeigt gewesen, bei denen der Virus zwar nur in geringem Maße tödlich war, aber bei bestehenden Vorerkrankungen oft eine Intensivmedizinische Versorgung notwendig war.
Viren konkurrieren untereinander – und Bakterien sind nicht unbeteiligt
Auffällig war, dass 2019/2020 Influenza kaum eine Rolle spielte. Nur 2% der Influenza-Erkrankten wiesen auch CoV2-Viren auf (RKI AG Influenza-Berichte). Leider wurde nicht untersucht, wie viele Covid-19-Patienten auch noch Influenza-Viren in sich tragen. Aus der Ökologie heraus wäre nur ein kleiner Anteil zu erwarten, da die ökologische Nische „Atemwege“ besetzt ist. Entweder von dem einen oder dem anderen Virus. Die Zahlen der von Corona-Viren Betroffenen wären unter diesem Aspekt einmal ins Verhältnis zu setzen mit den in anderen Jahren an bakteriellen und viralen Atemwegserkrankungen Verstorbenen, insbesondere aus den entsprechenden Risikogruppen. Es wäre eine vergleichbare Dynamik zu erwarten, die dann die Frage aufwerfen würde, ob überhaupt Menschenleben durch die Maßnahmen gerettet wurden. Die invasiven Pneumokokken haben in dieser Risikogruppe statistisch eine Letalität von ca. 30% – in diesem Sinne wäre für 2020 eine geringere Zahl der tödlich verlaufenden Pneumokokken-Infekte bei älteren Menschen zu erwarten.
Das Märchen von der sterilen Immunität
Neben der präventiven und therapeutischen antiviralen Strategie, sind Impfungen ein scheinbar erfolgsversprechendes Konzept. Dies ist bei schwerwiegenden und „singulären“ Erkrankungen ein durchaus geeigneter Ansatz, der jedoch auch einer „denkverbotsfreien Forschung und Diskussion“ bedarf. Gerade bei schweren epidemisch auftretenden viralen Erkrankungen (Pocken, Polio, Masern usw.) ist dies prinzipiell aber ein geeigneter Ansatz.
Bei Erkrankungen, bei denen mehrere Pathogene um den gleichen Ort konkurrieren (z.B. Lunge: ca. 90 unterschiedliche Pneumokokken-Stämme und ähnlich viele unterschiedliche Viren mit einem hohen Veränderungspotential in der äußeren Hülle) sinken die realistischen Erfolgsaussichten einer Impfung leider schnell. Damit schwinden auch die erhoffte Sicherheit und ein effektiver Schutz vor der nächsten Pandemie. Neue Virusoberflächen würden dann auch neue Impfstoffe bedeuten. In welcher Form durchimpfte Populationen die Virusmutationsvarianz beeinflussen, ist eine weitere Frage der ökologischen Interaktionen, die zumindest ansatzweise untersucht werden muss.
Zwei Fragen stehen immer wieder im Raum: Können Geimpfte doch erkranken und können Geimpfte die Krankheit weiterverbreiten? Schützen Antikörper vollständig und können so geschützte Menschen die Krankheit aber trotzdem weiterverbreiten? Die immer wieder postulierte „sterile Immunität“, d.h. der durch Antikörper geschützte Mensch vernichtet jede Bakterie, jedes Virus adhoc und kann es nicht weitergeben, bleibt wohl eher Wunschdenken als Realität und ließ sich bisher nur in sehr künstlichen Tiermodellen zeigen.
Es scheint das Gegenteil Realität zu sein: Das Robert Koch Institut schrieb zu der Frage, ob Geimpfte andere anstecken können: „Unabhängig von der Art des Impfstoffes kann es auch bei geimpften Personen zu einer Infektion mit dem Influenzavirus kommen. Häufig verlaufen solche Infektionen dann mit milderen Krankheitssymptomen oder völlig unbemerkt. In diesen Fällen können Influenzaviren ausgeschieden und auf Kontaktpersonen übertragen werden.“
Für die Masernimpfung liegen dazu ebenfalls wissenschaftliche Daten vor:
„Third, we assume that ifinfection occurs in vaccine responders, they are less infectious in the sense that they shed virus on average for a shorter duration albeit with the same intensity than unvaccinated naturally infected individuals.”
https://pubmed.ncbi.nlm.nih.gov/1058808
Dieses Problem wird bei allen sich über die Schleimhäute entwickelnden Infekten bestehen bleiben. Antikörper im Blut stellen erst die zweite Abwehrlinie dar. Das Schleimhaut-Immunsystem mit den Zellen der angeborenen Abwehr (Makrophagen, NK-Zellen usw.) ist die vorgelagerte erste Linie der Abwehr – diese muss zunächst überwunden werden. Denn erst wenn große Mengen Viren nach erfolgreichem Eindringen aus befallenen Schleimhaut-Zellen freigesetzt werden, beginnt die symptomatische Phase. Diese ganze erste Phase läuft völlig unabhängig von Antikörpern im Blut ab! Denn erst wenn die Viren ins Blut gelangen, können Antikörper die Viren abfangen und die Menge und die Verteilung eindämmen. Der Immunitätsausweis, der sich ja allein auf Antikörper z.B. nach einer möglichen Impfung beziehen würde, ist daher Augenwischerei.
Fazit
Unser Wissen über die Ausbreitung und Ansteckung von Viren ist derzeit sehr lückenhaft. Wie Viren es in kürzester Zeit schaffen um die Welt zu reisen ist unklar. Viren sind nichts anderes als in eine „Hülle“ verpackte Erbinformation, die wir in der inaktiven Form kaum nachweisen können.
Die Mechanismen, die Viren nutzen, um einen pandemischen Ausbruch von Krankheiten zu initiieren sind unbekannt, ebenso wie die unterschiedlichen Strategien, die virale Replikation zu starten und in die Phase einer aktiven krankheiterregenden Form einzutreten. Eine Verbreitung, u.U. auch schon in humanen Zellen, könnte dem Krankheitsprozess also weit vorauslaufen.
Die Rolle des menschlichen Viroms in der Abwehr oder als Triggerfaktor kann derzeit noch nicht einmal seriös abgeschätzt werden. Hierzu bedarf es eines wissenschaftlichen „Rundum-Blicks“. Der derzeitige Ansatz der medizinischen Virusforschung ist nur fokussiert auf die klinischen Übertragungswege, beschreibt die Pathogenität nur als Eigenschaft des Virus, hat die komplexe Wirt-Virus Interaktion nicht im Blick und sieht die Lösung nur in Impfung und antiviraler Medikation. Wir sind dabei, die Fehler der bakteriellen Infektiologie bei der Bekämpfung viraler Infektionen zu wiederholen. 700.000 Tote jährlich durch multiresistente Bakterien sollte uns eine Warnung sein.
Über den Autor
Dr. Uwe Peters studierte Biologie an der Universität Bochum und promovierte mit einem ökologischen Thema. Nach dem Studium arbeitete er zunächst für die Fa. Behring Marburg.
Seine weiter berufliche Laufbahn war und ist bestimmt durch die „Mikrobiologische Therapie“. Der berühmte Spruch „die Mikrobe ist nichts -das Terrain ist alles“ begleitet seine wissenschaftliche Auseinandersetzung mit dem Thema Darmbakterien und Schleimhautimmunität. In dieser Funktion ist er Mitglied des Arbeitskreises für Mikrobiologische Therapie (AMT e.V.). Er ist zudem Mitglied des wissenschaftlichen Beirats der medizinischen Enzymforschungsforschungsgesellschaft (MEF e.V.) und in der Association for natural medicine in Europe (ANME e.V.).
Bekannt ist er durch viele Vorträge und Webinare, wie die Nacht der Naturheilkunde und als Referent für die Zusatzbezeichnung „Naturheilverfahren“.

