Peter Chappells AIDS Remedy PC1
Unsere Feldstudie in Afrika ist publiziert
Hintergrundgeschichte
Ich fand abgedrehte Therapien schon immer interessant, und zwar deswegen, weil wissenschaftliche Innovationen und neue Erkenntnisse historisch gesehen sehr oft vom Rand des Mainstreams kamen und kommen. Nicht immer, aber sehr häufig. Daher habe ich mich seinerzeit mit Homöopathie beschäftigt, als mich Freunde und Kollegen während meiner Studienzeit in die legendären Homöopathievorlesungen von Dr. Köhler geschleppt haben. Damals dachte ich: Das ist so verrückt, wenn das stimmt, dann ist es ja revolutionär. Daraufhin habe ich mich mit Homöopathie wissenschaftlich beschäftigt. Ich habe einige Arzneimittelprüfungen durchgeführt und klinische Forschung gemacht und habe dann, nach ca. 10 Jahren intensiver Forschung, 3 Büchern [1-3], einer Reihe von peer-reviewten Arbeiten [4-10], ausführlicher Beschäftigung mit Placeboeffekten [11-15] festgestellt: Ja, irgendwas passiert da, das jenseits von zufälligen Schwankungen ist, das wir aber in keiner Weise verstehen und schon gar nicht mit den konventionell kausalen Wissenschaftsmodellen erklären können [16]. Ich habe versucht, das mit den momentan verfügbaren wissenschaftlichen Modellen greifbar zu machen, aber ob das wirklich zielführend ist, weiß ich noch immer nicht [17].
Während meine heiße Homöopathieforschungszeit Anfang der 2000er Jahre abkühlte, kam Harry van der Zee auf mich zu, ein holländischer homöopathischer Arzt. Er wollte unsere Kopfschmerzstudie nachmachen, aber besser als wir. Diese gehört zu den Studien in der homöopathischen Datenbank, die den mit Abstand schlechtesten Effekt für die Homöopathie gefunden hat [7, 10]. Ich habe Harry eingeladen. Wir verbrachten einige Tage gemeinsam und kochten das vermeintlich unschlagbare Design aus. Harry ging nach Hause, machte eine Pilotstudie, bei der das rauskam, was ich ihm prophezeite, nämlich nicht das, was er erwartet hatte. Und weil es keine Förderung gab, wurde am Ende nichts daraus.
Peter Chappell und PC1
Aber wir sind Freunde geblieben. Nach Jahren vermittelte er Peter Chappell den Kontakt zu mir. Peter Chappell, der letztes Jahr gestorben ist, war ein englischer Homöopath, der im früheren Leben als Elektroingenieur gearbeitet hat. Zu seinen Erfindungen gehörten Magnetstreifen an Plastikgeldkarten, wie er mir mal erzählte. Peter Chappell arbeitete einige Jahre als klassischer Homöopath und ging auch eine Weile nach Afrika, wo er Menschen mit AIDS behandelte. Dort kam ihm offenbar die Idee, dass man Homöopathie noch einfacher machen kann. Er sah sich die Totalität der Symptome eines Krankheitsbildes an, z. B. wie sich AIDS in Afrika zeigt. Und packte diese „Information“ in eine Flasche Wasser. Wie genau, sagte er nicht. Aber ich vermute mal, es ist einfach ein intentionaler Akt, bei dem mit großer Sammlung und Konzentration und schätzungsweise auch wohlwollend-heilender Intention diese „Information“ in eine Wasserflasche gebracht wird. Später erzählte er dann Freunden: Die Arzneimittel entstanden, indem er eine intensive Bitte an die „Quelle“ richtete, ein Simillimum, also ein homöopathisch möglichst passendes Arzneimittel, zu erzeugen. Diese „Quelle“ empfand er offenbar als eine Art transzendenter Wirklichkeit, die sowohl in als auch jenseits von ihm war.
Das hat viel Ähnlichkeit mit der Herstellung von Homöopathika und mit Bachblüten, nur dass bei Peter Chappell keine pharmazeutische Aufbereitung und kein Aufstellen von Blüten in der Sonne passierte, sondern alles rein intentional. Solche Heilmittel hat Peter Chappell für unterschiedliche Krankheiten entwickelt, aber das erste war das gegen AIDS in Afrika, PC1 (für Peter Chappell Arzneimittel 1).
AIDS in Afrika ist nämlich mehr als die Folge einer Infektion mit dem Retrovirus HIV. Es ist ein Sammelsurium von opportunistischen Infektionen, die vor allem auch auf dem Boden einer durch Mangel erzeugten Schwäche des Immunsystems gedeihen können und zum klinischen Bild von AIDS beitragen. Deswegen sage ich auch „AIDS in Afrika“, weil das gleiche Arzneimittel PC1 der Erfahrung nach bei AIDS-Kranken in den westlichen Ländern nicht so gut funktioniert. Aber in Afrika offenbar schon. Für AIDS in westlichen Ländern entwickelte Peter Chappell ein anderes Arzneimittel.
Amma Resonance Healing Foundation
In Afrika gab es schon seit den 2000er Jahren homöopathische Versorgungsstationen. Und die Amma-Resonance-Healing-Foundation (ARHF), die Harry van der Zee mittlerweile aufgebaut hat, verteilt dort das PC1 Heilmittel. Es wird in England und in Holland hergestellt, von der ARHF zum Selbstkostenpreis auf Spendenbasis eingekauft und in Afrika verteilt. Auf der Website der ARHF findet sich allerhand Information dazu, vor allem auch ein Film, der die konkrete Anwendung von PC1 in Afrika zeigt.
Aus dieser Logistik heraus entstand vor Jahren der Wunsch, die Wirksamkeit von PC1 zu evaluieren. Ich hatte an einer Planungstagung teilgenommen und zugesagt, die Daten auszuwerten – falls es denn einmal welche geben sollte – und auch geholfen, ein Forschungsprotokoll zu entwickeln. Und in der Tat erhielt ich vor einigen Jahren einen entsprechenden Datensatz, für dessen Richtigkeit Harry van der Zee einstand, der die Studie in Afrika vor Ort begleitet und gemonitort hat. Jetzt ist die Studie nach vielem Hin und Her endlich publiziert [18].
Die Studie
Weil es außer systematischen Fallbeschreibungen und Beobachtungen im Feld bislang keinerlei Daten gab, hatten sich Harry und sein Team dafür entschieden, eine naturalistische Studie zu organisieren, bei der sich die Gruppen aus den Wahlmöglichkeiten vor Ort ergaben. Es hat sich nämlich in Afrika herumgesprochen, dass die antiretroviralen Arzneimittel nicht immer gut verträglich sind und eine Reihe von Nebenwirkungen produzieren. Daher wollen manche diese Medikamente nicht nehmen. Ihnen wurde PC1 angeboten. Alle, die antiretrovirale Arzneien wollten, die erhielten sie auch. Und manche von denen wollten zusätzlich auch noch PC1, also das volle Programm.
Die Studie wurde in Kenia durchgeführt, einem Land, das weltweit die meisten AIDS-Fälle berichtet. Drei unterschiedliche, spezialisierte AIDS-Kliniken nahmen an der Untersuchung teil und brachten Patienten ein. Das Protokoll definierte, dass nur neu diagnostizierte AIDS-Patienten aufgenommen werden sollten, bei denen die Standard-Diagnostik (CD4-Count, Viral Load) zu Anfang gemacht wurde. Allen Patienten wurden antiretrovirale Medikamente (ARVs) angeboten. Die ARVs, die dort verteilt werden und wurden waren Abacavir, Lamuvidin und Efavirenz bei Kindern und Jugendlichen und bei älteren zusätzlich noch Tenofovir. In einer der drei Kliniken wurden entweder ARVs oder PC1 gegeben. In zwei Kliniken wurden den Patienten neben ARVs auch PC1 angeboten. In einer Klinik erhielten die Patienten ARVs. Dies war als Kontrolle gedacht. Nur wenn diese Patienten die ARVs ablehnten, erhielten sie nur PC1. Insofern haben wir hier also durchaus eine große Streuung der Behandlungsprotokolle und Kliniken.
PC1 wird wie ein Homöopathikum in größeren Flaschen bereitgehalten und mit der Flüssigkeit werden dann Globuli imprägniert. Für die Studie erhielten die Patienten eine 20ml Tropfflasche, in der ein Globulus PC1 in Mineralwasser mit 20 % medizinischem Alkohol gelöst war (der Alkohol ist nötig, um die Flüssigkeit zu konservieren und ungewollte Bakterienbildung zu vermeiden). Sie sollen jeweils einen Schluck pro Tag trinken und die Flasche vorher schütteln.
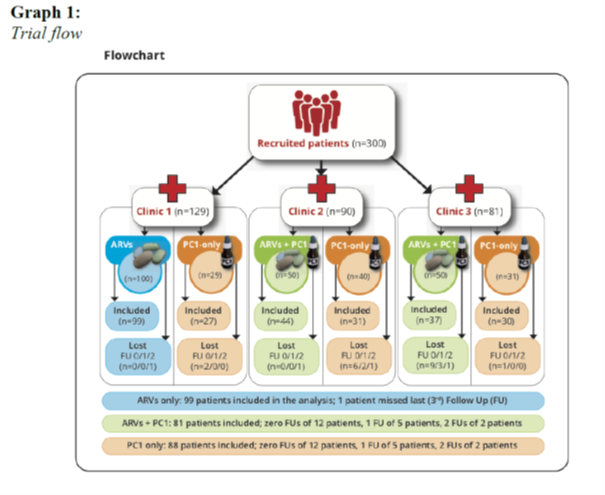
Die Studienorganisation und Patientenverteilung ist in der Grafik 1 dargestellt:

Insgesamt wurden 300 Patienten eingeschlossen, von denen 268 Patienten ausgewertet werden konnten. Von den anderen 32 fehlten die Daten. Das lag wohl daran, dass die Patienten regelmäßig zweimal pro Monat in die Klinik kommen mussten, um sich die Medikamente zu holen. Bei der Gelegenheit wurden auch die klinischen Daten erhoben und eingetragen. Die Patienten hatten dabei oft sehr weite Wege zurückzulegen. Teilweise waren diese durch Regen unpassierbar, und in manchen Landesteilen gab es offenbar auch Unruhen. Auch hatten manche Patienten falsche Telefonnummern und Adressen hinterlegt, sodass sie nicht mehr erreicht werden konnten. Aber ein Ausfall von ca. 10 % in einer Feldstudie in Afrika ist aus meiner Sicht ein gutes Ergebnis und spricht für die lokale Organisation.
Im Kenianischen Landesprotokoll ist vorgesehen, dass CD4-Count nur zu Beginn der Diagnosestellung gemessen wird und Viral Load alle 6 Monate. In dieser Studie wurde beides zu Beginn gemessen und auch nach 6 Monaten nochmals eine Blutprobe genommen und diese Parameter bestimmt. Außerdem wurden als klinische Parameter bei jedem Klinikbesuch Appetit, Gewichts-Zu- oder -Abnahme, Erschöpfung und Schwäche erfasst.
Die statistische Auswertung habe ich mit sehr robusten nicht-parametrischen Methoden vorgenommen. Das sind Methoden, die keine Verteilungsannahmen über die zugrundeliegende Datenverteilung machen und daher immer anwendbar. Die wichtigsten Daten fasse ich in Tabelle 1 zusammen; die vollen Daten sind in unserer Publikation einsehbar.
CD4-Count erhöhte sich unter PC1 mehr als in den anderen Gruppen, die virale Belastung verringerte sich. Auch die klinischen Parameter (Gewicht, Appetit, Erschöpfung, Schwäche) verbesserten sich deutlich und signifikant. Das Muster war eindeutig: Die Patienten in der PC1-Gruppe verbesserten sich in den objektiven Parametern mehr als die in der ARV+PC1 Gruppe, die wiederum besser waren als die Patienten in der ARV-Gruppe.
Man könnte nun vermuten, das hätte daran gelegen, dass die Patienten, die nur ARVs erhielten diejenigen mit der größeren Krankheitsbelastung waren. Das war aber nicht so, im Gegenteil: diejenigen, die nur ARVs erhielten waren anfangs klinisch weniger belastet, hatten bessere Ausgangsdaten in CD4-Count und Viral Load, während die Gruppe, die nur PC1 erhielt, diejenige mit den schlechtesten Ausgangswerten war (Originaltabelle in unserer Publikation).
| Nur ARVs | ARVs + PC1 | Nur PC1 | |
| CD4-Count Zunahme | 2,48 % | 7,37 % | 19,81 % |
| Viral Load Abnahme | 43,63 % | 43,61 % | 53,35 % |
| Gewichtszunahme | 3,28 % | 6,64 % | 8,44 % |
| Appetit (Differenz)* | 0,63 (0,92) | 1,10 (0,72) | 1,02 (0,88) |
| Erschöpfung (Differenz)* | 0,32 (0,7) | 1,30 (0,78) | 1,16 (0,84) |
| Schwäche (Differenz)* | 0,13 (0,66) | 1,07 (0,79) | 0,75 (0,97) |
Betrachtet man Tabelle 1, in der die Ergebnisvariablen wiedergegeben sind, dann sieht man: in den zentralen, weil objektiv gemessenen Parametern CD4-Count, Viral Load und Gewicht sind die Zunahmen unter PC1 deutlich größer als unter der Kombination ARV+PC1 oder nur ARV. Diese Effekte sind in der non-parametrischen statistischen Testung hoch-signifikant. Dieses Muster ist bei den klinischen Variablen leicht verändert, weil dort die Gruppe, die beide Medikamente erhalten hat, die größere Veränderung beschreibt. Aber auch hier ist die PC1-Gruppe der ARV-Gruppe weit überlegen. Wer sich meine Methodenblogs zur Effektstärkeberechnung angesehen hat (https://harald-walach.de/methodenlehre-fuer-anfaenger/13-power-analyse-die-magie-der-statistik-oder-der-unterschied-zwischen-signifikanz-und-relevanz/ https://harald-walach.de/methodenlehre-fuer-anfaenger/14-die-magie-der-statistik-in-aktion-tamiflu-der-groesste-raub-der-geschichte-ziemlich-unbrauchbar/ https://harald-walach.de/23-wie-funktionieren-meta-analysen-eigentlich/), kann jetzt die Mittelwertdifferenz durch die Standardabweichung teilen und erhält die Effektgröße d. Diese Effektgrößen liegen bei den klinischen Variablen für ARVs zwischen 0,19 und 0,78, für ARVs+PC1 bei 1,1 bis 1,78, für PC1 bei 0,6 bis 1,5.
Die Effektgrößen sind also für die aktiven Gruppen ARV+PC1 bzw. PC1 klinisch groß bis sehr groß und damit auf jeden Fall bedeutsam. Für die ARV-Gruppe sind sie immer noch relativ groß, aber deutlich kleiner.
Dies zeigt in der Summe: PC1 ist offenbar ARVs nicht nur nicht unterlegen, sondern deutlich überlegen. Anscheinend ist eine Kombination dieser beiden Behandlungen auch klinisch sinnvoll.
Diese Daten muss man natürlich auf dem Hintergrund ihrer möglichen Probleme betrachten.
Mögliche Fehlerquellen
Diese Studie war naturalistisch. Das heißt, das Zustandekommen der Gruppen ist durch Wahl der Patienten und/oder Ärzte geschehen, jedenfalls nicht zufällig. Das bedeutet, die beobachteten Effekte könnten natürlich auch durch noch nicht weiter beschriebene Drittvariable zustande gekommen sein. Dass es daran lag, dass die Patienten in der PC1 Gruppe weniger schwer krank waren, ist wie gesagt sehr unwahrscheinlich. Denn die klinischen Werte dieser Gruppe waren in allen erfassten Parametern schlechter. Es könnte höchstens sein, dass deswegen bei der zweiten Messung die Werte stärker vom Erwartungswert abwichen, also eine statistische Regression zu Mitte stattfand. Aber mir scheint, dass eine derart große und konsistente Abweichung eher nicht durch ein statistisches Artefakt erklärbar ist. Zumal bei 32 Patienten der PC1-Gruppe auch noch ein Ein-Jahres-Followup gemacht wurde, das die positive Tendenz bestätigt. Denn dort ging die Verbesserung weiter.
Auch die mangelnde Verblindung ist ein Manko dieser Studie. Dadurch, dass Patienten und Behandler wussten, wer wie behandelt wurde, kann es gut sein, dass eine Verzerrung vorkam. Diese könnte zugunsten von PC1 wirken, nämlich dann, wenn Patienten oder Behandler von der Behandlung positiv eingenommen sind. Sie könnte aber natürlich auch anders wirken. Wir wissen es einfach nicht. Dagegen spricht allerdings, dass die Laborwerte in Laboren analysiert wurden, die von der Behandlung keine Ahnung hatten und daher einfach Messungen durchführten, die praktisch verblindet waren. Ein Hinweis auf Verzerrung scheinen mir die größeren Effektstärken der Gruppe ARV+PC1 ausschließlich bei den klinischen Parametern zu sein. Denn diese wurden offen erhoben und dort wussten alle, dass die Patienten zwei Behandlungen erhielten. Zwei ist ja bekanntlich mehr als eine Behandlung. Also bessere Werte.
Spitzfindige könnten jetzt kommen und sagen: immerhin haben die Leute in der PC1 Gruppe ein maulvoll mehr Wasser am Tag getrunken als die anderen. Eher unwahrscheinlich. Denn es handelte sich um 5 Tropfen pro Tag. Müsste man vielleicht in einer guten Studie auch kontrollieren. Aber das wäre dann die ultimative Blamage für ARVs, wenn ein maulvoll Wasser besser wäre als diese.
Und spitzfindigen Statistikfüchsen sei gesagt: Multiples Testen ist nicht das Problem. Ich habe zwar Tests für insgesamt sechs Variablen gemacht. Aber die Signifikanzniveaus waren so hoch, ich hätte ein ganzes Bataillon von Variablen testen können und die Signifikanz wäre auch nach Korrektur für 100 Variablen noch geblieben. Siehe die Originalpublikation.
Störvariablen sind bei naturalistischen Studien nicht auszuschließen. Daher würde nur eine randomisierte Studie, die von Anfang an alle Patienten per Zufall zuweist, Sicherheit bringen. Dafür liegen nun die entsprechenden Informationen vor. Man kann hoffen, dass die Planer dieser Studie eine Möglichkeit finden, diese Daten in einer methodisch sauberen randomisierten Studie erhärten.
Intention in der Flasche – Conflict of Interest Statement
Anscheinend, so zeigt diese Studie, kann man eine therapeutische Intention in Flaschen abfüllen und verteilen, zum Wohle derer, denen sie nützen soll. Nebenwirkungen wurden auf jeden Fall nicht beobachtet und sind auch bei früheren Beobachtungen nie berichtet worden.
Bleibt noch zu erwähnen: Alle Beteiligten, Harry van der Zee, Peter Chappell und ich arbeiten in diesem Kontext ohne Gewinnabsichten. Ich habe meine Zeit unentgeltlich zur Verfügung gestellt, auch Harry. Die Arzneimittel werden von einer Apotheke hergestellt, der die Amma Resonance Healing Foundation sie abkauft und kostenfrei in Afrika verteilt. Dies geschieht mittels Spenden. Das Personal, das vor Ort für die Studie gearbeitet hat, wurde vom Staat finanziert. Die Ethikkommission der University of Northampton, wo ich damals war, hat diese Studie geprüft und als ethisch unproblematisch eingestuft.
Wir haben also einen negativen Conflict of Interest. Wenn sich diese Behandlung in Afrika durchsetzt oder in weiteren Studien als wirkungsvoll erweist, dann kriegen wir Haue von denen, denen die ARV-Felle davonschwimmen. Aber das bin ich ja schon gewöhnt.
Quellen und Literatur
- Walach, H., Wissenschaftliche Homöopathische Arzneimittelprüfung. Doppelblinde Crossover-Studie einer homöopathischen Hochpotenz gegen Placebo. 1992, Heidelberg: Haug.
- Walach, H., Homöopathie als Basistherapie. Plädoyer für die wissenschaftliche Ernsthaftigkeit der Homöopathie. 1986, Heidelberg: Haug.
- Walach, H., Wissenschaftliche Untersuchungen zur Homöopathie. Die Münchener Kopfschmerzstudie -Arzneimittelprüfungen mit Belladonna. 2000, Essen: KVC Verlag.
- Walach, H., Die Untersuchung der Homöopathie durch das Reichsgesundheitsamt 1936 – 1939. Zeitschrift für Klassische Homöopathie, 1990. 34: p. 252-259.
- Walach, H., et al., Research on homeopathy: State of the art. Journal of Alternative and Complementary Medicine, 2005. 11: p. 813-829.
- Walach, H., et al., The effects of homeopathic belladonna 30CH in healthy volunteers – a randomized, double-blind experiment. Journal of Psychosomatic Research, 2001. 50: p. 155-160.
- Walach, H., et al., The long-term effects of homeopathic treatment of chronic headaches: One year follow-up. Cephalalgia, 2000. 20: p. 835-837.
- Walach, H., Homoeopathy as Semiotic. Semiotica, 1991. 83: p. 81-95.
- Walach, H., Does a highly diluted homoeopathic drug act as a placebo in healthy volunteers? Experimental study of Belladonna C30. Journal of Psychosomatic Research, 1993. 37: p. 851-860.
- Walach, H., et al., Classical homoeopathic treatment of chronic headaches. A double-blind, randomized, placebo-controlled study. Cephalalgia, 1997. 17: p. 119-126.
- Walach, H. and W.B. Jonas, Placebo research: The evidence base for harnessing self-healing capacities. Journal of Alternative and Complementary Medicine, 2004. 10(Suppl. 1): p. S103-S112.
- Walach, H., et al., Homeopathic proving symptoms: result of a local,non-local, or placebo process? A blinded, placebo-controlled pilot study. Homeopathy, 2004. 93: p. 179-185.
- Walach, H., Placebo and placebo effects – a concise review. Focus on Alternative and Complementary Therapies, 2003. 8: p. 178-187.
- Walach, H. and C. Sadaghiani, Plazebo und Plazebo-Effekte: Eine Bestandsaufnahme. Psychotherapie, Psychosomatik, medizinische Psychologie, 2002. 52: p. 332-342.
- Walach, H., The efficacy paradox in randomized controlled trials of CAM and elsewhere: Beware of the placebo trap. Journal of Alternative & Complementary Medicine, 2001. 7: p. 213-218.
- Walach, H., Magic of signs: a non-local interpretation of homeopathy. British Homeopathic Journal, 2000. 89: p. 127-140.
- Walach, H., Entanglement model of homeopathy as an example of generalizsed entanglement predicted by Weak Quantum Theory. Forschende Komplementärmedizin und Klassische Naturheilkunde, 2003. 10: p. 192-200.
- van der Zee, H. and H. Walach, Novel immune supportive treatment of HIV/AIDS: comparative outcomes study in rural clinics in Africa. International Journal of Healing and Caring, 2024. 24(1): p. 18-43.